دیستروفی عضلانی لیمب گیردل Limb Girdle Muscular Dystrophy (LGMD) نام مجموعه ای متنوع از اختلالات عصبی عضلانی با علل ژنتیکی مختلف است.
کمربند اندامی ساختار استخوانی اطراف مفصل شانه و لگن است.
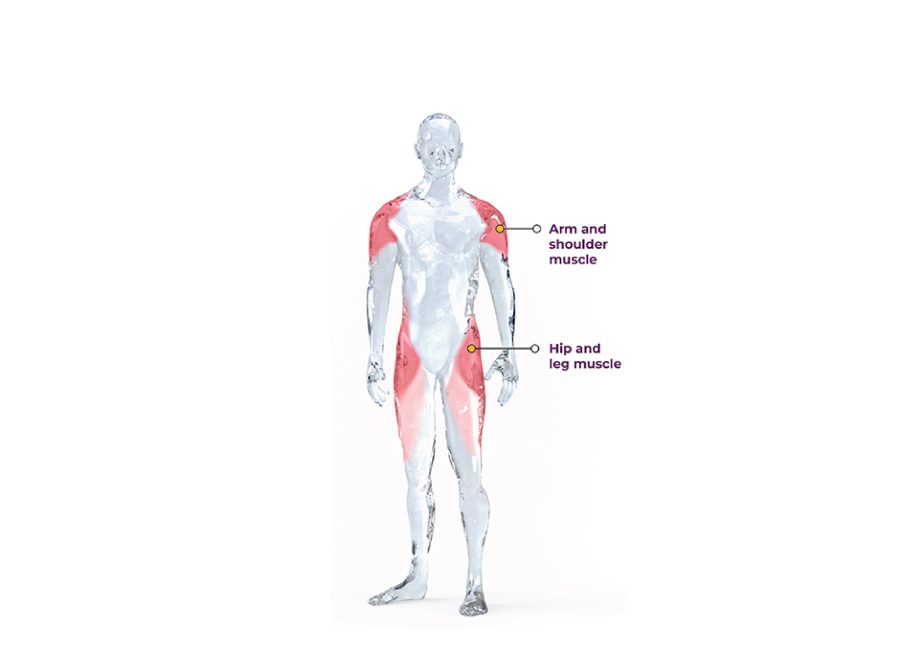
دیستروفی عضلانی لیمب گیردل با آتروفی عضلانی در نواحی کمربند بدن یا در عضلات اطراف شانه ها و باسن مشخص می شود.
برآورد میزان بروز LGMD از یک در 14،500 تا یک در 123،000 نفر متغیر است.
در نتیجه با استفاده از این آمار و در نظر گرفتن جمعیت 85 میلیون نفری ایران آماری تقریبا حدود 691 تا 5862 نفر در ایران امکان دارد به این بیماری مبتلا باشند.
لیمب گیردل Limb Girdle Muscular Dystrophy (LGMD) بر اساس الگوی وراثت این اختلال به دو گروه
LGMD1 و LGMD2 تقسیم می شود.
LGMD1 به صورت اتوزومی غالب به ارث می رسد ، به این معنی که تنها یک نسخه از ژن معیوب برای ظهور بیماری کافی است.
از طرف دیگر ، LGMD2 به صورت اتوزوم مغلوب به ارث می رسد ، به این معنی که هر دو نسخه از ژن عامل
– یکی از هر یک از والدین به ارث رسیده است – باید جهش داشته باشند تا بیماری ایجاد شود.
LGMD می تواند در هر سنی ایجاد شود. در مراحل اولیه بیماری ، بیماران ممکن است راه رفتن غیرمعمول داشته باشند ،
در دویدن مشکل داشته باشند ، بیشتر زمین بخورند و بعد از نشستن روی زمین با ایستادن مشکل داشته باشند.
ضعف عضلانی معمولاً ابتدا در شانه ها ظاهر می شود ، در حالی که تیغه های شانه برای ایجاد جلوه بالدار بیرون آمده اند.
آتروفی بیشتر ماهیچه ها در اطراف کمربند شانه ای باعث می شود که بیماران نتوانند بازوهای خود را به حالت کشیده یا بالا در هوا نگه دارند.
کاردیومیوپاتی یا آتروفی عضله قلب ، برخی از اشکال LGMD را تحت تأثیر قرار می دهد.
همچنین بیماران در معرض ضعف عضلات دیافراگم مورد نیاز برای تنفس هستند.
این علائم شدیدتر با انواع خاصی از LGMD همراه است.
LGMD به راحتی با انواع دیگر شرایط تحلیل رفتن ماهیچه اشتباه گرفته می شود.
با توجه به وجود بیش از 30 نوع دیستروفی عضلانی لیمب گیردل، تشخیص می تواند مشکل باشد.
پس از معاینه فیزیکی و بررسی سابقه خانوادگی ، پزشک ممکن است برای تأیید تشخیص ،
بیوپسی عضلانی یا آزمایش الکترومیوگرافی درخواست کند.
تنها راه تشخیص بیمار با نوع خاصی از LGMD آزمایش ژنتیکی است.
در حال حاضر هیچ درمانی برای LGMD وجود ندارد ، اما درمان های موجود می تواند به بیماران در مدیریت علائم بیماری کمک کند.
برنامه های درمانی باید برای هر بیمار طراحی شود ، زیرا ممکن است نوع متفاوتی از LGMD و در نتیجه علائم خاص را داشته باشد.
پزشکان معمولاً فیزیوتراپی و وسایل کمکی ارتوپدی – احتمالاً شامل ویلچر – را برای بیماران LGMD پیشنهاد می کنند.