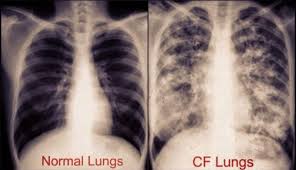
 شایع ترین اختلال اتوزومی مغلوب در کودکان اروپایی 1 در هر 2500 تولد است. فیبروز کیستی با میزان بروز 1 مورد در هر 3200 تولد زنده در ایالات متحده، فراوانترین بیماری کشنده ژنتیکی است که جمعیت قفقازی را مبتلا میکند. در حدود یک نفر از هر 25 نفر در ایالات متحده ی آمریکا حامل هترو زیگوت برای الل جهش یافته ی سیستیک فیبروزیس است. این بیماری در بین آسیایی ها 1مورد در 32000 تولد زنده و آمریکایی های آفریقایی تبار 1 مورد در 15000 تولد زنده ناشایع است.فراوانی CF در بین متولدین سفید پوست برابر با 1به25000است. فراوانی حاملین CFبرابر با 1 به 25 است. اگر هم مادر و هم پدر ازخانوادهای باشندکه فیبروز کیستیک در آن وجود داشته است ، شانس بروز بی ماری در کودک آنها 1به 4است.علت بیماری نوزاد از بدو تولد این بیماری را از پدر و مادر خود به ارث می برد. اگر پدر و مادر هر دو سالم باشند اما هر یک از آنها حامل یک ژن معیوب فیبروز کیستی باشند هر فرزندی را که مادر حامله شود 25درصد شانس به ارث بردن هر دو ژن معیوب و در نتیجه ابتلاء به فیبروز کیستی را دارد علت اصلی این بیماری، نقص در ژن کدکننده پروتئین RTFC است .علایم ناشی از بیماری ترشحات غیر طبیعی از علایم اصلی این اختلال است که شدیدترین اثر آن در سیستم تنفسی است که موکوس چسبنده ای به صورت غیر طبیعی راه های طبیعی هوایی را مسدود می کند. مژک هایی که نایژه ها را مفروش می کنند به آسانی نمی توانند موکوس را بر دارند بنابراین به محیطی برای رشد باکتری های خطرناک تبدیل می شوند. این باکتری ها یا سموم آن ها به بافتهای اطراف آسیب رسانده و منجر به ذات الریه عود کننده و مشکلات دیگری می شوند در این حالت، غده های برونشی بجای تولید مخاط رقیق طبیعی، خلط غلیظ و لزجی تولید می کنند که منجر به بسته شدن مجاری عبور هوا میشود و در نهایت عفونتهای ریوی را بوجود میآورد و وقتیکه بخشهایکوچکی از ریهها فرسوده شوند خطر ذات الریه را به همراه دارد. این عارضه اخیر و عفونتهای عود کننده در مبتلایان به فیبروزکیستی شایع است .عفونتهای عود کننده همراه با سرفه و ناراحتیهای تنفسی اسهال، ممکن است بصورت دوره ای با یبوست جایش را عوض کند. مدفوع چرب و بدبو نارسایی رشد ورم شکم و تحلیل رفتن دستها و پاها .در رودههای کودک مبتلا به فیبروز کیستی ،لوزالمعده نمی تواند برخی آنزیمهای حیاتی را تولید کند .این آنزیمها به عمل هضم کمک و غذا را شکسته و تجزیه میکنند تا بدن بتواند آنها را آسانتر جذب کند. فقدان این آنزیم های هضم کننده بدان معنا است که غذا بدرستی جذب نمیشود و موجب اسهال و مدفوع بدبو می گردد. از آنجائیکه غذا جذب نمیشود بدن بسیاری از مواد غذایی ضروری را که برای سلامتی لازم است دریافت نمیکند در نتیجه ،کودک رشد نمیکند و همچنان کوچک و کم وزن باقی میماند ممکن است بعد از هر دوره اسهال، یبوست جایگزین آن شود و توالی این مطلب میتواند عملاً روده را مسدود کند.روش تشخیص اگر چه آزمایشهای ساده ای روی خون و مدفوع نوزادان می توان انجام داد اما آزمایش قطعی برای فیبروز کیستی تست عرق می باشد زیرا میزان نمک عرق در این بیماران بالا است در مورد برادران و خواهران فرد مبتلا و در نوزادانی که دچار مراحل عود کننده ذات الریه هستند و دچار توقف رشد شده اند نیز این آزمایش انجام میگیرد. تهیه نمونه ها از مایع آمنیون و خون با استفاده از روش های روتین استخراج ژنوم و بررسی برای یافتن یکی از رایج ترین جهش ها در ژن CF با استفاده از روش 1RFLP انجام میگیرد.درمان درمان های کنونی برای سیستیک فیبروزیس( CF)عموما جهت تسکین علایم بیماران هستند. آنتی بیوتی کها برای کنترل عفونتهای باکتریایی مورد استفاده قرار می گیرند اما درمان فیزیکی روزانه برای پاک کردن موک وسها از سیستم تنفسی مورد نیاز است.به دلیل بروز عفونت های باکتریایی مزمن و کشنده در راههای تنفسی کنترل عفونتو حفظ عملکرد تنفسی مطلوب کلید اصلی درمان است.دارو درمانی در این بیماران شامل موارد زیر است:آنتی بیوتیک ها به منظور پیشگیری از عفونت استفاده می شوند .داروهای گشاد کننده برونش برای باز نگه داشتن مسیرهای تنفسی استفاده میشود.از کورتون ها به منظور کاهش التهاب در سیستم تنفسی استفاده میگردد.برحسب نیاز از آنزیمهای پانکراس(لوزالمعده) برای کاهش مشکلات گوارشی استفاده میشود.مکمل های ویتامین های محلول در چربی برای بیمار تجویز میشود که معمولا به صورت روزانه مصرف میشود.زمانی که کودک در بیمارستان بستری است یا در موارد بیماری ریوی پیشرفته برای پیشگیری از کمبود اکسیژن ممکن است اکسیژن درمانی انجام شود .مراقبت های لازم رویکرد تیمی برای کم ک به مراقب ت از کودک(درمانگر تنفسی، پرستار، متخصص تغذیه، فیریوتراپ ،مشاور، مددکار اجتماعی)تا جایی که میتوانید اطلاعات خود را در مورد این بیماری بالا ببرید. توجه داشته باشید که رژیم غذایی ، دارو، و تشخیص زودهنگام عفونت بسیار مهم هستند.تخلیه روزانه مخاط ریه ها با تغییر وضعی ت بدن و نیز ضربه زدن به قفسه سی نه برای تکان دادن و نرم کردن تکه های مخاطی چسبنا ک، در بهبود علایم ظاهری بیمار مؤثر خواهد بود .هر گاه کود ک علایم تنفسی دارد ،از دستگاه بخور استفاده کنید. رطوبت به ناز ک کردن مخاط کمک می کند و بنابراین مخاط راحت تر با سرفه خارج می شود. دستگاه بخور را هر روز تمیز کنید .واکسیناسیون کودک خود را به روز نگاه دارید. کودک باید واکسن آنفلوانزا نیز دریافت کند .کودک خود را تشویق کنید تا زندگی طبیعی و فعال داشته باشد .پیوند ریه نیز تدریجاً به جرگه روشهای درمانی پیوسته است.پیش آگهیتغییرات آناتومیک در CF بسیار متغییر هستند و به این بستگی دارد که کدام غده و با چه شدتی درگیر شده است.اختلالات پانکراسی در تقریبا 85 تا 90 درصد بیماران مبتلا به CF وجود دارد. در موارد خفیف تر فقط تجمع موکوس در مجاری کوچک اتساع یافته غدد اگزو کرین وجود دارد. در موارد پیشرفته تر که معمولا در بچه های بزرگتر یا نوجوانان دیده میشود، مجاری کاملا مسدود شده اند که این حالت باعث آتروفی غدد برون ریز و فیبروز پیشرونده میگردد. آزواسپرمی و ناباروری در 95 درصد مردانی که تا بزرگسالی زنده می مانند دیده می شود.فقدان دو طرفه وازودفران یافته ی شایعی در این بیماران می باشد این بی ماری در حال حاضر علاج ناپذیر است و غالباً بیمار در همان بچگی فوت می کند. مراقبت دقیق و درازمدت توسط والدین و تیم پزشکی به کودک کمک می کند تا زندگی تقریباً راحتی داشته باشد. البته کودکانی که دچار انواع خفیف تر بیماری هستند تا دوران بزرگسالی زنده می مانند ،خصوصاً اگر این بیماری زود تشخیص داده شود .میانگین طول عمر بیماران 28 سال است . محققان ژن مسؤول بیماری فیبروز کیستیک را کشف کرده اند. هم اکنون در مورد روش های نوین پیشگیری و درمان این بیماری کارهای زیادی در حال انجام است.
شایع ترین اختلال اتوزومی مغلوب در کودکان اروپایی 1 در هر 2500 تولد است. فیبروز کیستی با میزان بروز 1 مورد در هر 3200 تولد زنده در ایالات متحده، فراوانترین بیماری کشنده ژنتیکی است که جمعیت قفقازی را مبتلا میکند. در حدود یک نفر از هر 25 نفر در ایالات متحده ی آمریکا حامل هترو زیگوت برای الل جهش یافته ی سیستیک فیبروزیس است. این بیماری در بین آسیایی ها 1مورد در 32000 تولد زنده و آمریکایی های آفریقایی تبار 1 مورد در 15000 تولد زنده ناشایع است.فراوانی CF در بین متولدین سفید پوست برابر با 1به25000است. فراوانی حاملین CFبرابر با 1 به 25 است. اگر هم مادر و هم پدر ازخانوادهای باشندکه فیبروز کیستیک در آن وجود داشته است ، شانس بروز بی ماری در کودک آنها 1به 4است.علت بیماری نوزاد از بدو تولد این بیماری را از پدر و مادر خود به ارث می برد. اگر پدر و مادر هر دو سالم باشند اما هر یک از آنها حامل یک ژن معیوب فیبروز کیستی باشند هر فرزندی را که مادر حامله شود 25درصد شانس به ارث بردن هر دو ژن معیوب و در نتیجه ابتلاء به فیبروز کیستی را دارد علت اصلی این بیماری، نقص در ژن کدکننده پروتئین RTFC است .علایم ناشی از بیماری ترشحات غیر طبیعی از علایم اصلی این اختلال است که شدیدترین اثر آن در سیستم تنفسی است که موکوس چسبنده ای به صورت غیر طبیعی راه های طبیعی هوایی را مسدود می کند. مژک هایی که نایژه ها را مفروش می کنند به آسانی نمی توانند موکوس را بر دارند بنابراین به محیطی برای رشد باکتری های خطرناک تبدیل می شوند. این باکتری ها یا سموم آن ها به بافتهای اطراف آسیب رسانده و منجر به ذات الریه عود کننده و مشکلات دیگری می شوند در این حالت، غده های برونشی بجای تولید مخاط رقیق طبیعی، خلط غلیظ و لزجی تولید می کنند که منجر به بسته شدن مجاری عبور هوا میشود و در نهایت عفونتهای ریوی را بوجود میآورد و وقتیکه بخشهایکوچکی از ریهها فرسوده شوند خطر ذات الریه را به همراه دارد. این عارضه اخیر و عفونتهای عود کننده در مبتلایان به فیبروزکیستی شایع است .عفونتهای عود کننده همراه با سرفه و ناراحتیهای تنفسی اسهال، ممکن است بصورت دوره ای با یبوست جایش را عوض کند. مدفوع چرب و بدبو نارسایی رشد ورم شکم و تحلیل رفتن دستها و پاها .در رودههای کودک مبتلا به فیبروز کیستی ،لوزالمعده نمی تواند برخی آنزیمهای حیاتی را تولید کند .این آنزیمها به عمل هضم کمک و غذا را شکسته و تجزیه میکنند تا بدن بتواند آنها را آسانتر جذب کند. فقدان این آنزیم های هضم کننده بدان معنا است که غذا بدرستی جذب نمیشود و موجب اسهال و مدفوع بدبو می گردد. از آنجائیکه غذا جذب نمیشود بدن بسیاری از مواد غذایی ضروری را که برای سلامتی لازم است دریافت نمیکند در نتیجه ،کودک رشد نمیکند و همچنان کوچک و کم وزن باقی میماند ممکن است بعد از هر دوره اسهال، یبوست جایگزین آن شود و توالی این مطلب میتواند عملاً روده را مسدود کند.روش تشخیص اگر چه آزمایشهای ساده ای روی خون و مدفوع نوزادان می توان انجام داد اما آزمایش قطعی برای فیبروز کیستی تست عرق می باشد زیرا میزان نمک عرق در این بیماران بالا است در مورد برادران و خواهران فرد مبتلا و در نوزادانی که دچار مراحل عود کننده ذات الریه هستند و دچار توقف رشد شده اند نیز این آزمایش انجام میگیرد. تهیه نمونه ها از مایع آمنیون و خون با استفاده از روش های روتین استخراج ژنوم و بررسی برای یافتن یکی از رایج ترین جهش ها در ژن CF با استفاده از روش 1RFLP انجام میگیرد.درمان درمان های کنونی برای سیستیک فیبروزیس( CF)عموما جهت تسکین علایم بیماران هستند. آنتی بیوتی کها برای کنترل عفونتهای باکتریایی مورد استفاده قرار می گیرند اما درمان فیزیکی روزانه برای پاک کردن موک وسها از سیستم تنفسی مورد نیاز است.به دلیل بروز عفونت های باکتریایی مزمن و کشنده در راههای تنفسی کنترل عفونتو حفظ عملکرد تنفسی مطلوب کلید اصلی درمان است.دارو درمانی در این بیماران شامل موارد زیر است:آنتی بیوتیک ها به منظور پیشگیری از عفونت استفاده می شوند .داروهای گشاد کننده برونش برای باز نگه داشتن مسیرهای تنفسی استفاده میشود.از کورتون ها به منظور کاهش التهاب در سیستم تنفسی استفاده میگردد.برحسب نیاز از آنزیمهای پانکراس(لوزالمعده) برای کاهش مشکلات گوارشی استفاده میشود.مکمل های ویتامین های محلول در چربی برای بیمار تجویز میشود که معمولا به صورت روزانه مصرف میشود.زمانی که کودک در بیمارستان بستری است یا در موارد بیماری ریوی پیشرفته برای پیشگیری از کمبود اکسیژن ممکن است اکسیژن درمانی انجام شود .مراقبت های لازم رویکرد تیمی برای کم ک به مراقب ت از کودک(درمانگر تنفسی، پرستار، متخصص تغذیه، فیریوتراپ ،مشاور، مددکار اجتماعی)تا جایی که میتوانید اطلاعات خود را در مورد این بیماری بالا ببرید. توجه داشته باشید که رژیم غذایی ، دارو، و تشخیص زودهنگام عفونت بسیار مهم هستند.تخلیه روزانه مخاط ریه ها با تغییر وضعی ت بدن و نیز ضربه زدن به قفسه سی نه برای تکان دادن و نرم کردن تکه های مخاطی چسبنا ک، در بهبود علایم ظاهری بیمار مؤثر خواهد بود .هر گاه کود ک علایم تنفسی دارد ،از دستگاه بخور استفاده کنید. رطوبت به ناز ک کردن مخاط کمک می کند و بنابراین مخاط راحت تر با سرفه خارج می شود. دستگاه بخور را هر روز تمیز کنید .واکسیناسیون کودک خود را به روز نگاه دارید. کودک باید واکسن آنفلوانزا نیز دریافت کند .کودک خود را تشویق کنید تا زندگی طبیعی و فعال داشته باشد .پیوند ریه نیز تدریجاً به جرگه روشهای درمانی پیوسته است.پیش آگهیتغییرات آناتومیک در CF بسیار متغییر هستند و به این بستگی دارد که کدام غده و با چه شدتی درگیر شده است.اختلالات پانکراسی در تقریبا 85 تا 90 درصد بیماران مبتلا به CF وجود دارد. در موارد خفیف تر فقط تجمع موکوس در مجاری کوچک اتساع یافته غدد اگزو کرین وجود دارد. در موارد پیشرفته تر که معمولا در بچه های بزرگتر یا نوجوانان دیده میشود، مجاری کاملا مسدود شده اند که این حالت باعث آتروفی غدد برون ریز و فیبروز پیشرونده میگردد. آزواسپرمی و ناباروری در 95 درصد مردانی که تا بزرگسالی زنده می مانند دیده می شود.فقدان دو طرفه وازودفران یافته ی شایعی در این بیماران می باشد این بی ماری در حال حاضر علاج ناپذیر است و غالباً بیمار در همان بچگی فوت می کند. مراقبت دقیق و درازمدت توسط والدین و تیم پزشکی به کودک کمک می کند تا زندگی تقریباً راحتی داشته باشد. البته کودکانی که دچار انواع خفیف تر بیماری هستند تا دوران بزرگسالی زنده می مانند ،خصوصاً اگر این بیماری زود تشخیص داده شود .میانگین طول عمر بیماران 28 سال است . محققان ژن مسؤول بیماری فیبروز کیستیک را کشف کرده اند. هم اکنون در مورد روش های نوین پیشگیری و درمان این بیماری کارهای زیادی در حال انجام است. سیستیک فیبروزیس (Cystic Fibrosis)
 شایع ترین اختلال اتوزومی مغلوب در کودکان اروپایی 1 در هر 2500 تولد است. فیبروز کیستی با میزان بروز 1 مورد در هر 3200 تولد زنده در ایالات متحده، فراوانترین بیماری کشنده ژنتیکی است که جمعیت قفقازی را مبتلا میکند. در حدود یک نفر از هر 25 نفر در ایالات متحده ی آمریکا حامل هترو زیگوت برای الل جهش یافته ی سیستیک فیبروزیس است. این بیماری در بین آسیایی ها 1مورد در 32000 تولد زنده و آمریکایی های آفریقایی تبار 1 مورد در 15000 تولد زنده ناشایع است.فراوانی CF در بین متولدین سفید پوست برابر با 1به25000است. فراوانی حاملین CFبرابر با 1 به 25 است. اگر هم مادر و هم پدر ازخانوادهای باشندکه فیبروز کیستیک در آن وجود داشته است ، شانس بروز بی ماری در کودک آنها 1به 4است.علت بیماری نوزاد از بدو تولد این بیماری را از پدر و مادر خود به ارث می برد. اگر پدر و مادر هر دو سالم باشند اما هر یک از آنها حامل یک ژن معیوب فیبروز کیستی باشند هر فرزندی را که مادر حامله شود 25درصد شانس به ارث بردن هر دو ژن معیوب و در نتیجه ابتلاء به فیبروز کیستی را دارد علت اصلی این بیماری، نقص در ژن کدکننده پروتئین RTFC است .علایم ناشی از بیماری ترشحات غیر طبیعی از علایم اصلی این اختلال است که شدیدترین اثر آن در سیستم تنفسی است که موکوس چسبنده ای به صورت غیر طبیعی راه های طبیعی هوایی را مسدود می کند. مژک هایی که نایژه ها را مفروش می کنند به آسانی نمی توانند موکوس را بر دارند بنابراین به محیطی برای رشد باکتری های خطرناک تبدیل می شوند. این باکتری ها یا سموم آن ها به بافتهای اطراف آسیب رسانده و منجر به ذات الریه عود کننده و مشکلات دیگری می شوند در این حالت، غده های برونشی بجای تولید مخاط رقیق طبیعی، خلط غلیظ و لزجی تولید می کنند که منجر به بسته شدن مجاری عبور هوا میشود و در نهایت عفونتهای ریوی را بوجود میآورد و وقتیکه بخشهایکوچکی از ریهها فرسوده شوند خطر ذات الریه را به همراه دارد. این عارضه اخیر و عفونتهای عود کننده در مبتلایان به فیبروزکیستی شایع است .عفونتهای عود کننده همراه با سرفه و ناراحتیهای تنفسی اسهال، ممکن است بصورت دوره ای با یبوست جایش را عوض کند. مدفوع چرب و بدبو نارسایی رشد ورم شکم و تحلیل رفتن دستها و پاها .در رودههای کودک مبتلا به فیبروز کیستی ،لوزالمعده نمی تواند برخی آنزیمهای حیاتی را تولید کند .این آنزیمها به عمل هضم کمک و غذا را شکسته و تجزیه میکنند تا بدن بتواند آنها را آسانتر جذب کند. فقدان این آنزیم های هضم کننده بدان معنا است که غذا بدرستی جذب نمیشود و موجب اسهال و مدفوع بدبو می گردد. از آنجائیکه غذا جذب نمیشود بدن بسیاری از مواد غذایی ضروری را که برای سلامتی لازم است دریافت نمیکند در نتیجه ،کودک رشد نمیکند و همچنان کوچک و کم وزن باقی میماند ممکن است بعد از هر دوره اسهال، یبوست جایگزین آن شود و توالی این مطلب میتواند عملاً روده را مسدود کند.روش تشخیص اگر چه آزمایشهای ساده ای روی خون و مدفوع نوزادان می توان انجام داد اما آزمایش قطعی برای فیبروز کیستی تست عرق می باشد زیرا میزان نمک عرق در این بیماران بالا است در مورد برادران و خواهران فرد مبتلا و در نوزادانی که دچار مراحل عود کننده ذات الریه هستند و دچار توقف رشد شده اند نیز این آزمایش انجام میگیرد. تهیه نمونه ها از مایع آمنیون و خون با استفاده از روش های روتین استخراج ژنوم و بررسی برای یافتن یکی از رایج ترین جهش ها در ژن CF با استفاده از روش 1RFLP انجام میگیرد.درمان درمان های کنونی برای سیستیک فیبروزیس( CF)عموما جهت تسکین علایم بیماران هستند. آنتی بیوتی کها برای کنترل عفونتهای باکتریایی مورد استفاده قرار می گیرند اما درمان فیزیکی روزانه برای پاک کردن موک وسها از سیستم تنفسی مورد نیاز است.به دلیل بروز عفونت های باکتریایی مزمن و کشنده در راههای تنفسی کنترل عفونتو حفظ عملکرد تنفسی مطلوب کلید اصلی درمان است.دارو درمانی در این بیماران شامل موارد زیر است:آنتی بیوتیک ها به منظور پیشگیری از عفونت استفاده می شوند .داروهای گشاد کننده برونش برای باز نگه داشتن مسیرهای تنفسی استفاده میشود.از کورتون ها به منظور کاهش التهاب در سیستم تنفسی استفاده میگردد.برحسب نیاز از آنزیمهای پانکراس(لوزالمعده) برای کاهش مشکلات گوارشی استفاده میشود.مکمل های ویتامین های محلول در چربی برای بیمار تجویز میشود که معمولا به صورت روزانه مصرف میشود.زمانی که کودک در بیمارستان بستری است یا در موارد بیماری ریوی پیشرفته برای پیشگیری از کمبود اکسیژن ممکن است اکسیژن درمانی انجام شود .مراقبت های لازم رویکرد تیمی برای کم ک به مراقب ت از کودک(درمانگر تنفسی، پرستار، متخصص تغذیه، فیریوتراپ ،مشاور، مددکار اجتماعی)تا جایی که میتوانید اطلاعات خود را در مورد این بیماری بالا ببرید. توجه داشته باشید که رژیم غذایی ، دارو، و تشخیص زودهنگام عفونت بسیار مهم هستند.تخلیه روزانه مخاط ریه ها با تغییر وضعی ت بدن و نیز ضربه زدن به قفسه سی نه برای تکان دادن و نرم کردن تکه های مخاطی چسبنا ک، در بهبود علایم ظاهری بیمار مؤثر خواهد بود .هر گاه کود ک علایم تنفسی دارد ،از دستگاه بخور استفاده کنید. رطوبت به ناز ک کردن مخاط کمک می کند و بنابراین مخاط راحت تر با سرفه خارج می شود. دستگاه بخور را هر روز تمیز کنید .واکسیناسیون کودک خود را به روز نگاه دارید. کودک باید واکسن آنفلوانزا نیز دریافت کند .کودک خود را تشویق کنید تا زندگی طبیعی و فعال داشته باشد .پیوند ریه نیز تدریجاً به جرگه روشهای درمانی پیوسته است.پیش آگهیتغییرات آناتومیک در CF بسیار متغییر هستند و به این بستگی دارد که کدام غده و با چه شدتی درگیر شده است.اختلالات پانکراسی در تقریبا 85 تا 90 درصد بیماران مبتلا به CF وجود دارد. در موارد خفیف تر فقط تجمع موکوس در مجاری کوچک اتساع یافته غدد اگزو کرین وجود دارد. در موارد پیشرفته تر که معمولا در بچه های بزرگتر یا نوجوانان دیده میشود، مجاری کاملا مسدود شده اند که این حالت باعث آتروفی غدد برون ریز و فیبروز پیشرونده میگردد. آزواسپرمی و ناباروری در 95 درصد مردانی که تا بزرگسالی زنده می مانند دیده می شود.فقدان دو طرفه وازودفران یافته ی شایعی در این بیماران می باشد این بی ماری در حال حاضر علاج ناپذیر است و غالباً بیمار در همان بچگی فوت می کند. مراقبت دقیق و درازمدت توسط والدین و تیم پزشکی به کودک کمک می کند تا زندگی تقریباً راحتی داشته باشد. البته کودکانی که دچار انواع خفیف تر بیماری هستند تا دوران بزرگسالی زنده می مانند ،خصوصاً اگر این بیماری زود تشخیص داده شود .میانگین طول عمر بیماران 28 سال است . محققان ژن مسؤول بیماری فیبروز کیستیک را کشف کرده اند. هم اکنون در مورد روش های نوین پیشگیری و درمان این بیماری کارهای زیادی در حال انجام است.
شایع ترین اختلال اتوزومی مغلوب در کودکان اروپایی 1 در هر 2500 تولد است. فیبروز کیستی با میزان بروز 1 مورد در هر 3200 تولد زنده در ایالات متحده، فراوانترین بیماری کشنده ژنتیکی است که جمعیت قفقازی را مبتلا میکند. در حدود یک نفر از هر 25 نفر در ایالات متحده ی آمریکا حامل هترو زیگوت برای الل جهش یافته ی سیستیک فیبروزیس است. این بیماری در بین آسیایی ها 1مورد در 32000 تولد زنده و آمریکایی های آفریقایی تبار 1 مورد در 15000 تولد زنده ناشایع است.فراوانی CF در بین متولدین سفید پوست برابر با 1به25000است. فراوانی حاملین CFبرابر با 1 به 25 است. اگر هم مادر و هم پدر ازخانوادهای باشندکه فیبروز کیستیک در آن وجود داشته است ، شانس بروز بی ماری در کودک آنها 1به 4است.علت بیماری نوزاد از بدو تولد این بیماری را از پدر و مادر خود به ارث می برد. اگر پدر و مادر هر دو سالم باشند اما هر یک از آنها حامل یک ژن معیوب فیبروز کیستی باشند هر فرزندی را که مادر حامله شود 25درصد شانس به ارث بردن هر دو ژن معیوب و در نتیجه ابتلاء به فیبروز کیستی را دارد علت اصلی این بیماری، نقص در ژن کدکننده پروتئین RTFC است .علایم ناشی از بیماری ترشحات غیر طبیعی از علایم اصلی این اختلال است که شدیدترین اثر آن در سیستم تنفسی است که موکوس چسبنده ای به صورت غیر طبیعی راه های طبیعی هوایی را مسدود می کند. مژک هایی که نایژه ها را مفروش می کنند به آسانی نمی توانند موکوس را بر دارند بنابراین به محیطی برای رشد باکتری های خطرناک تبدیل می شوند. این باکتری ها یا سموم آن ها به بافتهای اطراف آسیب رسانده و منجر به ذات الریه عود کننده و مشکلات دیگری می شوند در این حالت، غده های برونشی بجای تولید مخاط رقیق طبیعی، خلط غلیظ و لزجی تولید می کنند که منجر به بسته شدن مجاری عبور هوا میشود و در نهایت عفونتهای ریوی را بوجود میآورد و وقتیکه بخشهایکوچکی از ریهها فرسوده شوند خطر ذات الریه را به همراه دارد. این عارضه اخیر و عفونتهای عود کننده در مبتلایان به فیبروزکیستی شایع است .عفونتهای عود کننده همراه با سرفه و ناراحتیهای تنفسی اسهال، ممکن است بصورت دوره ای با یبوست جایش را عوض کند. مدفوع چرب و بدبو نارسایی رشد ورم شکم و تحلیل رفتن دستها و پاها .در رودههای کودک مبتلا به فیبروز کیستی ،لوزالمعده نمی تواند برخی آنزیمهای حیاتی را تولید کند .این آنزیمها به عمل هضم کمک و غذا را شکسته و تجزیه میکنند تا بدن بتواند آنها را آسانتر جذب کند. فقدان این آنزیم های هضم کننده بدان معنا است که غذا بدرستی جذب نمیشود و موجب اسهال و مدفوع بدبو می گردد. از آنجائیکه غذا جذب نمیشود بدن بسیاری از مواد غذایی ضروری را که برای سلامتی لازم است دریافت نمیکند در نتیجه ،کودک رشد نمیکند و همچنان کوچک و کم وزن باقی میماند ممکن است بعد از هر دوره اسهال، یبوست جایگزین آن شود و توالی این مطلب میتواند عملاً روده را مسدود کند.روش تشخیص اگر چه آزمایشهای ساده ای روی خون و مدفوع نوزادان می توان انجام داد اما آزمایش قطعی برای فیبروز کیستی تست عرق می باشد زیرا میزان نمک عرق در این بیماران بالا است در مورد برادران و خواهران فرد مبتلا و در نوزادانی که دچار مراحل عود کننده ذات الریه هستند و دچار توقف رشد شده اند نیز این آزمایش انجام میگیرد. تهیه نمونه ها از مایع آمنیون و خون با استفاده از روش های روتین استخراج ژنوم و بررسی برای یافتن یکی از رایج ترین جهش ها در ژن CF با استفاده از روش 1RFLP انجام میگیرد.درمان درمان های کنونی برای سیستیک فیبروزیس( CF)عموما جهت تسکین علایم بیماران هستند. آنتی بیوتی کها برای کنترل عفونتهای باکتریایی مورد استفاده قرار می گیرند اما درمان فیزیکی روزانه برای پاک کردن موک وسها از سیستم تنفسی مورد نیاز است.به دلیل بروز عفونت های باکتریایی مزمن و کشنده در راههای تنفسی کنترل عفونتو حفظ عملکرد تنفسی مطلوب کلید اصلی درمان است.دارو درمانی در این بیماران شامل موارد زیر است:آنتی بیوتیک ها به منظور پیشگیری از عفونت استفاده می شوند .داروهای گشاد کننده برونش برای باز نگه داشتن مسیرهای تنفسی استفاده میشود.از کورتون ها به منظور کاهش التهاب در سیستم تنفسی استفاده میگردد.برحسب نیاز از آنزیمهای پانکراس(لوزالمعده) برای کاهش مشکلات گوارشی استفاده میشود.مکمل های ویتامین های محلول در چربی برای بیمار تجویز میشود که معمولا به صورت روزانه مصرف میشود.زمانی که کودک در بیمارستان بستری است یا در موارد بیماری ریوی پیشرفته برای پیشگیری از کمبود اکسیژن ممکن است اکسیژن درمانی انجام شود .مراقبت های لازم رویکرد تیمی برای کم ک به مراقب ت از کودک(درمانگر تنفسی، پرستار، متخصص تغذیه، فیریوتراپ ،مشاور، مددکار اجتماعی)تا جایی که میتوانید اطلاعات خود را در مورد این بیماری بالا ببرید. توجه داشته باشید که رژیم غذایی ، دارو، و تشخیص زودهنگام عفونت بسیار مهم هستند.تخلیه روزانه مخاط ریه ها با تغییر وضعی ت بدن و نیز ضربه زدن به قفسه سی نه برای تکان دادن و نرم کردن تکه های مخاطی چسبنا ک، در بهبود علایم ظاهری بیمار مؤثر خواهد بود .هر گاه کود ک علایم تنفسی دارد ،از دستگاه بخور استفاده کنید. رطوبت به ناز ک کردن مخاط کمک می کند و بنابراین مخاط راحت تر با سرفه خارج می شود. دستگاه بخور را هر روز تمیز کنید .واکسیناسیون کودک خود را به روز نگاه دارید. کودک باید واکسن آنفلوانزا نیز دریافت کند .کودک خود را تشویق کنید تا زندگی طبیعی و فعال داشته باشد .پیوند ریه نیز تدریجاً به جرگه روشهای درمانی پیوسته است.پیش آگهیتغییرات آناتومیک در CF بسیار متغییر هستند و به این بستگی دارد که کدام غده و با چه شدتی درگیر شده است.اختلالات پانکراسی در تقریبا 85 تا 90 درصد بیماران مبتلا به CF وجود دارد. در موارد خفیف تر فقط تجمع موکوس در مجاری کوچک اتساع یافته غدد اگزو کرین وجود دارد. در موارد پیشرفته تر که معمولا در بچه های بزرگتر یا نوجوانان دیده میشود، مجاری کاملا مسدود شده اند که این حالت باعث آتروفی غدد برون ریز و فیبروز پیشرونده میگردد. آزواسپرمی و ناباروری در 95 درصد مردانی که تا بزرگسالی زنده می مانند دیده می شود.فقدان دو طرفه وازودفران یافته ی شایعی در این بیماران می باشد این بی ماری در حال حاضر علاج ناپذیر است و غالباً بیمار در همان بچگی فوت می کند. مراقبت دقیق و درازمدت توسط والدین و تیم پزشکی به کودک کمک می کند تا زندگی تقریباً راحتی داشته باشد. البته کودکانی که دچار انواع خفیف تر بیماری هستند تا دوران بزرگسالی زنده می مانند ،خصوصاً اگر این بیماری زود تشخیص داده شود .میانگین طول عمر بیماران 28 سال است . محققان ژن مسؤول بیماری فیبروز کیستیک را کشف کرده اند. هم اکنون در مورد روش های نوین پیشگیری و درمان این بیماری کارهای زیادی در حال انجام است. 


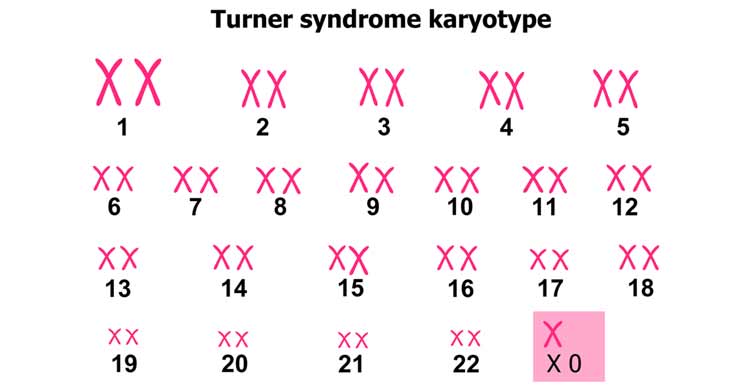 شیوع و همه گیری شناسی
این بیماری در ایالات متحده 1 مورد در هر 2000-2500 تولد مشاهده می شود یعنی حدود 800 مورد جدید تشخیصی در سال. در ایلات متحده در 75-80% موارد تک کروموزوم X از تخم مادر به جنین منتقل و اسپرم پدر که با تخم لقاح می یابد فاقد کروموزوم جنسی است.صرفا تعداد کمی بارداری در بین آن دسته از مبتلایان به TS که بطور خودبخود خونریزی قاعدگی داشته اند، گزارش شده است .3/1 فرزندان حاصله، دچار ناهنجاریهای مادرزادی مانند بیماری مادرزادی قلب، سندرم داون و ستون فقرات دو شاخه بوده اند .علت بیماری سندرم ترنر، اختلالی است که در تمام نژادها دیده می شود و ناشی از فقدان کامل یا نسبی کروموزوم x دوم در خانمهاست مونوزومی برای کروموزوم x بر اثر ناتوانی در گنجاندن یک کروموزوم x در یکی از گامتها یا از دست رفتن یک کروموزوم جنسی از گامت یا مراحل اولیه رویانی ایجاد میشود .علت بروز سندرم ترنر، رخداد “عدم انفصال” است. در طی تقسیم میتوز در هر والد رویداد عدم انفصال کروموزوم رخ داده که طی آن گامت یا اووسیت یا اسپرماتوسیت نه کروموزوم ایکس و نه کروموزوم y دارند. حال اگر این گامت ها با گامت والد دیگر لقاح یابد (کروموزوم نرمال دارد). رویان تشکیل شده دارای 45کروموزوم بوده و مونوزومی رخ میدهد.علایم ناشی از بیماری این افراد ظاهر کاملا زنانه دارند و با عدم وجود تخمدان( gonadal dysgenesi )وقد کوتاه مشخص می شوند. بیماران اغلب به سایر ناهنجاریهای مادرزادی مانند مشکلات آئورت، انسداد شریان ریوی، ناهنجاری های کلیوی، عقب ماندگی ذهنی و مشکلات شنوایی مبتلا هستند. سایر علایم بیماری عبارتند از :وجود بخشی پرده مانند در قسمت پوست بین گردن و شانهخط رویش موی پایین در پشت سرشکل غیر عادی چشمها از جمله افتادگی پلکادِِم لنفاوی اندام هانا هنجاری های اسکلتیسینه پهن و فاصله بیش از حد نوک پستان ها.تمام بیماران مبتلا به TS، کوتاه قد می باشند و بیش از 90 درصد آنها دیس ژنی تخمدان دارند. افراد دچار اختلال هوشی، معمولا واجد نوعی اختلال ساختمانی کروموزوم x هستند. از نظر اجتماعی، مبتلایان به TS معمولا خجالتی و منزوی هستند.روش تشخیص در نیمی از موارد تشخیص در ماههای اول زندگی به وسیله مشخصات فیزیکی صورت میگیرد. در سایر بیماران در دوران نوجوانی به علت رشد پایین تر از حد نرمال یا عدم رسیدن به بلوغ صورت میگیرد.زمانی که پزشک به سندرم ترنر مشکوک میشود میتواند با انجام کاریو تایپ (آنالیز کروموزوم) تشخیص را به طورقطعی تایید کند. سندرم ترنر می تواند در طول حاملگی به وسیله CVS یا آمینیو سنتز (نمونه گیری از مایع رحمی) مشخص شود.تشخیص این سندرم قبل از تولد جنین به واسطه آمینوسنتز امکان پذیر است و حتی ناهنجاریهای قلبی و کلیوی نیز با انجام سونوگرافی مشهود میگردد. اما این سندرم معمولا در ابتدای تولد و یا هنگامیکه انتظار میرود که بلوغ رخ داده باشد، تشخیص داده میشود .اگر کودک دارای چندین نشانه از سندرم ترنر باشد، آزمایش خون صورت گرفته و کاریوتیپ صورت می گیرد. این تست تعداد کروموزومهای فرد را شمارش کرده و هر گونه تغییر شکل ناهنجار و یا فقدان هر بخش از کروموزوم را تشخیص میدهد. در برخی موارد هیچ گونه علائم بالینی در ابتدای تولد مشهود نمی باشد و این امر تا رسیدن به زمان بلوغ دختر به تعویق می افتد. با این حال مهم است که این سندرم زودتر تشخیص داده شود تا هر چه زودتر درمانهای هورمونی لازم صورت گیرد. تشخیص زودرس و درمان به پیشگیری از سایر مشکلات بخصوص عوارض مزمن از قبیل استئوپورز و دیابت کمک خواهد کرد. استفاده متناوب از اولتراسوند می تواند در تعیین بیماری به وسیله نشانه های فیزیکی قبل از تولد کمک نماید .درمان تزریق هورمون رشد اگر به موقع انجام شود، می تواند با افزایش رشد، حداکثر قد در دوران بلوغ را افزایش دهد. درمان با استروژن معمولاً در سنین 12 یا 13 سال آغاز می شود و می تواند در بروز خصوصیات ثانویه جنسی موثر باشد اما نمی تواند موجب درمان نازایی شود. امروزه به زنان مبتلا به TS کمک می کنند که باردار شوند. به این ترتیب که یک تخمک اهدایی بارور شده را پرورش داده و رویان را در رحم بیمار ترنری جاسازی می کنند. به کمک هورمون درمانی، این زن می تواند جنین آزمایشگاهی را حفظ نموده و زایمان کند.مراقبت های لازم بسیار ضروری است که دختر خود را برای معالجه به نزد پزشک خانوادگی و یا متخصص اطفال برده و او را تحت معاینه و مداوا قرار دهید. زیرا که پزشک او در طول زندگی بیمار هماهنگی لازم برای انجام سایر خدمات را در میان تعدادی از متخصصان به وجود می آورد.معاینات منظم پیشرفت های قابل توجهی در کیفیت و طول عمر زنان مبتلا به سندرم را به وجود آورده است.عادات زندگی سالم، حفظ وزن مناسب و ورزش منظم در طول زندگی مهم هستند. در طول این دوره مشاوره با متخصص قلب و حصول اطمینان از سلامت بافت قلبی و فعالیت آن اهمیت دارد. پیش آگهی این ناهنجاری کروموزومی با مشکلات و عوارض بسیاری همراه است علاوه بر فقدان بلوغ جنسی اگر نقص قلبی شدیدی برای نوزاد مبتلا به سندرم ترنر حادث نشده باشد بسیاری از دختران مبتلا تا دوران بزرگسالی زنده می مانند. در حدود 2 تا 5 درصد زنان مبتلا به این سندرم، دارای مشکلات تخمدانی هستند. مبتلایان به این سندرم ممکن است در آینده از عوارضی مانند ناهنجاری های کلیه، فشار خون بالا، چاقی، دیابت، کاتاراکت، آرتریت و اسکلیوزیس رنج ببرند.
شیوع و همه گیری شناسی
این بیماری در ایالات متحده 1 مورد در هر 2000-2500 تولد مشاهده می شود یعنی حدود 800 مورد جدید تشخیصی در سال. در ایلات متحده در 75-80% موارد تک کروموزوم X از تخم مادر به جنین منتقل و اسپرم پدر که با تخم لقاح می یابد فاقد کروموزوم جنسی است.صرفا تعداد کمی بارداری در بین آن دسته از مبتلایان به TS که بطور خودبخود خونریزی قاعدگی داشته اند، گزارش شده است .3/1 فرزندان حاصله، دچار ناهنجاریهای مادرزادی مانند بیماری مادرزادی قلب، سندرم داون و ستون فقرات دو شاخه بوده اند .علت بیماری سندرم ترنر، اختلالی است که در تمام نژادها دیده می شود و ناشی از فقدان کامل یا نسبی کروموزوم x دوم در خانمهاست مونوزومی برای کروموزوم x بر اثر ناتوانی در گنجاندن یک کروموزوم x در یکی از گامتها یا از دست رفتن یک کروموزوم جنسی از گامت یا مراحل اولیه رویانی ایجاد میشود .علت بروز سندرم ترنر، رخداد “عدم انفصال” است. در طی تقسیم میتوز در هر والد رویداد عدم انفصال کروموزوم رخ داده که طی آن گامت یا اووسیت یا اسپرماتوسیت نه کروموزوم ایکس و نه کروموزوم y دارند. حال اگر این گامت ها با گامت والد دیگر لقاح یابد (کروموزوم نرمال دارد). رویان تشکیل شده دارای 45کروموزوم بوده و مونوزومی رخ میدهد.علایم ناشی از بیماری این افراد ظاهر کاملا زنانه دارند و با عدم وجود تخمدان( gonadal dysgenesi )وقد کوتاه مشخص می شوند. بیماران اغلب به سایر ناهنجاریهای مادرزادی مانند مشکلات آئورت، انسداد شریان ریوی، ناهنجاری های کلیوی، عقب ماندگی ذهنی و مشکلات شنوایی مبتلا هستند. سایر علایم بیماری عبارتند از :وجود بخشی پرده مانند در قسمت پوست بین گردن و شانهخط رویش موی پایین در پشت سرشکل غیر عادی چشمها از جمله افتادگی پلکادِِم لنفاوی اندام هانا هنجاری های اسکلتیسینه پهن و فاصله بیش از حد نوک پستان ها.تمام بیماران مبتلا به TS، کوتاه قد می باشند و بیش از 90 درصد آنها دیس ژنی تخمدان دارند. افراد دچار اختلال هوشی، معمولا واجد نوعی اختلال ساختمانی کروموزوم x هستند. از نظر اجتماعی، مبتلایان به TS معمولا خجالتی و منزوی هستند.روش تشخیص در نیمی از موارد تشخیص در ماههای اول زندگی به وسیله مشخصات فیزیکی صورت میگیرد. در سایر بیماران در دوران نوجوانی به علت رشد پایین تر از حد نرمال یا عدم رسیدن به بلوغ صورت میگیرد.زمانی که پزشک به سندرم ترنر مشکوک میشود میتواند با انجام کاریو تایپ (آنالیز کروموزوم) تشخیص را به طورقطعی تایید کند. سندرم ترنر می تواند در طول حاملگی به وسیله CVS یا آمینیو سنتز (نمونه گیری از مایع رحمی) مشخص شود.تشخیص این سندرم قبل از تولد جنین به واسطه آمینوسنتز امکان پذیر است و حتی ناهنجاریهای قلبی و کلیوی نیز با انجام سونوگرافی مشهود میگردد. اما این سندرم معمولا در ابتدای تولد و یا هنگامیکه انتظار میرود که بلوغ رخ داده باشد، تشخیص داده میشود .اگر کودک دارای چندین نشانه از سندرم ترنر باشد، آزمایش خون صورت گرفته و کاریوتیپ صورت می گیرد. این تست تعداد کروموزومهای فرد را شمارش کرده و هر گونه تغییر شکل ناهنجار و یا فقدان هر بخش از کروموزوم را تشخیص میدهد. در برخی موارد هیچ گونه علائم بالینی در ابتدای تولد مشهود نمی باشد و این امر تا رسیدن به زمان بلوغ دختر به تعویق می افتد. با این حال مهم است که این سندرم زودتر تشخیص داده شود تا هر چه زودتر درمانهای هورمونی لازم صورت گیرد. تشخیص زودرس و درمان به پیشگیری از سایر مشکلات بخصوص عوارض مزمن از قبیل استئوپورز و دیابت کمک خواهد کرد. استفاده متناوب از اولتراسوند می تواند در تعیین بیماری به وسیله نشانه های فیزیکی قبل از تولد کمک نماید .درمان تزریق هورمون رشد اگر به موقع انجام شود، می تواند با افزایش رشد، حداکثر قد در دوران بلوغ را افزایش دهد. درمان با استروژن معمولاً در سنین 12 یا 13 سال آغاز می شود و می تواند در بروز خصوصیات ثانویه جنسی موثر باشد اما نمی تواند موجب درمان نازایی شود. امروزه به زنان مبتلا به TS کمک می کنند که باردار شوند. به این ترتیب که یک تخمک اهدایی بارور شده را پرورش داده و رویان را در رحم بیمار ترنری جاسازی می کنند. به کمک هورمون درمانی، این زن می تواند جنین آزمایشگاهی را حفظ نموده و زایمان کند.مراقبت های لازم بسیار ضروری است که دختر خود را برای معالجه به نزد پزشک خانوادگی و یا متخصص اطفال برده و او را تحت معاینه و مداوا قرار دهید. زیرا که پزشک او در طول زندگی بیمار هماهنگی لازم برای انجام سایر خدمات را در میان تعدادی از متخصصان به وجود می آورد.معاینات منظم پیشرفت های قابل توجهی در کیفیت و طول عمر زنان مبتلا به سندرم را به وجود آورده است.عادات زندگی سالم، حفظ وزن مناسب و ورزش منظم در طول زندگی مهم هستند. در طول این دوره مشاوره با متخصص قلب و حصول اطمینان از سلامت بافت قلبی و فعالیت آن اهمیت دارد. پیش آگهی این ناهنجاری کروموزومی با مشکلات و عوارض بسیاری همراه است علاوه بر فقدان بلوغ جنسی اگر نقص قلبی شدیدی برای نوزاد مبتلا به سندرم ترنر حادث نشده باشد بسیاری از دختران مبتلا تا دوران بزرگسالی زنده می مانند. در حدود 2 تا 5 درصد زنان مبتلا به این سندرم، دارای مشکلات تخمدانی هستند. مبتلایان به این سندرم ممکن است در آینده از عوارضی مانند ناهنجاری های کلیه، فشار خون بالا، چاقی، دیابت، کاتاراکت، آرتریت و اسکلیوزیس رنج ببرند. 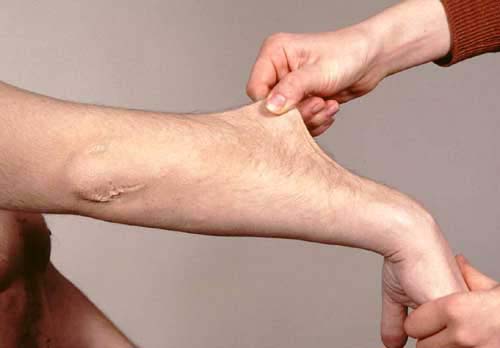
 میزان شیوع این بیماری از 1 در250000تا 1 در 50000در جمعیت عمومی برآورد شده است. اما مطالعات صورت گرفته در مناطق وسیع تر حاکی از افزایش آمار این بیماری است و محققان معتقدند گستره این بیماری وسیع تر از آمار برآورد شده می باشد چرا که تنوع این بیماری بیشتر است. سندرم اهلر دانلوس در تمام قومها و نژادها بین زنان و مردان به نسبت مساوی شایع است .هر چند بعضی از انواع آن در بین گروههای خاصی رایج ترند.علت بیماری انواع مختلفی از این سندرم بر پایه نوع تغییری است که در ژنهای فرد رخ داده است. مهمترین چالشی که در این سندرم وجود دارد ،پروتئین های فیبری هستند که باعث الاستیسیته و استحکام بافت همبند میگردد. این موتاسیون ژنتیکی باعث تغییر در عملکرد آنزیمی میگردد که فقدان آن باعث ضعف و ناپایداری بافت همبند میگردد. بیشترین فرم ابتلا به این سندرم در اثر حالتی رخ می دهد که به “الگوی اتوزومال غالب” معروف است. این بدان معناست که برای ابتلا به این سندرم تنها وجود یک کپی از این ژن ناقص کافی خواهد بود. در این صورت احتمال 50 درصد وجود دارد که کودکی به این سندرم مبتلا گردد و این ژن جهش یافته را به ارث ببرد .علایم ناشی از بیماری علائم و نشانه های رایج این سندرم عبارتند از:انعطاف زیاد و یا شکنندگی پوستروند غیر نرمال ترمیم زخم که بیش از حد معمول زمان لازم دارندانعطاف پذیری بیش از حد مفاصل که دامنه حرکتی بیش از حد نرمال خود دارند.در رفتگی، شانه، هیپ، زانو و انگشتانضعف ماهیچه ایتاخیر تکامل حرکتیکبود شدگی پوستمشکلات قلبی و گسیختگی خودبخودی دیواره عروقسابقه خانوادگی، آنوریسم مغزی و یا کولونروش تشخیص تشخیص این سندرم بر پایه، یافتههای بالینی بیماران و سابقه خانوادگی آنان می باشد. در برخی از انواع این سندرم بیوپسی پوست به منظور بررسی ترکیبات شیمیایی بافتهای همبند مورد استفاده قرار میگیرد.تستهای ژنتیکی: تست DNA برای انواع کلاسیک، عروقی، کیفواسکلیوزیس، مورد استفاده قرار میگیرد.تست ادراری: این تست برای تشخیص فرم کیفواسکلیوز موثر خواهد بود. این تست میزان آنزیمی که به واسطه بروز این فرم از سندرم تولید می شود را اندازه گیری میکند.بیوپسی پوست: در این تست مقداری نمونه پوستی گرفته و در زیر میکروسکپ مورد بررسی قرار می گیرد. این تست به تشخیص ناهنجاریهایی در ساختار فیبری پوست مفید خواهد بود .اولتراسوند قلبی: بررسی به منظور تشخیص پرولاپس میترال
میزان شیوع این بیماری از 1 در250000تا 1 در 50000در جمعیت عمومی برآورد شده است. اما مطالعات صورت گرفته در مناطق وسیع تر حاکی از افزایش آمار این بیماری است و محققان معتقدند گستره این بیماری وسیع تر از آمار برآورد شده می باشد چرا که تنوع این بیماری بیشتر است. سندرم اهلر دانلوس در تمام قومها و نژادها بین زنان و مردان به نسبت مساوی شایع است .هر چند بعضی از انواع آن در بین گروههای خاصی رایج ترند.علت بیماری انواع مختلفی از این سندرم بر پایه نوع تغییری است که در ژنهای فرد رخ داده است. مهمترین چالشی که در این سندرم وجود دارد ،پروتئین های فیبری هستند که باعث الاستیسیته و استحکام بافت همبند میگردد. این موتاسیون ژنتیکی باعث تغییر در عملکرد آنزیمی میگردد که فقدان آن باعث ضعف و ناپایداری بافت همبند میگردد. بیشترین فرم ابتلا به این سندرم در اثر حالتی رخ می دهد که به “الگوی اتوزومال غالب” معروف است. این بدان معناست که برای ابتلا به این سندرم تنها وجود یک کپی از این ژن ناقص کافی خواهد بود. در این صورت احتمال 50 درصد وجود دارد که کودکی به این سندرم مبتلا گردد و این ژن جهش یافته را به ارث ببرد .علایم ناشی از بیماری علائم و نشانه های رایج این سندرم عبارتند از:انعطاف زیاد و یا شکنندگی پوستروند غیر نرمال ترمیم زخم که بیش از حد معمول زمان لازم دارندانعطاف پذیری بیش از حد مفاصل که دامنه حرکتی بیش از حد نرمال خود دارند.در رفتگی، شانه، هیپ، زانو و انگشتانضعف ماهیچه ایتاخیر تکامل حرکتیکبود شدگی پوستمشکلات قلبی و گسیختگی خودبخودی دیواره عروقسابقه خانوادگی، آنوریسم مغزی و یا کولونروش تشخیص تشخیص این سندرم بر پایه، یافتههای بالینی بیماران و سابقه خانوادگی آنان می باشد. در برخی از انواع این سندرم بیوپسی پوست به منظور بررسی ترکیبات شیمیایی بافتهای همبند مورد استفاده قرار میگیرد.تستهای ژنتیکی: تست DNA برای انواع کلاسیک، عروقی، کیفواسکلیوزیس، مورد استفاده قرار میگیرد.تست ادراری: این تست برای تشخیص فرم کیفواسکلیوز موثر خواهد بود. این تست میزان آنزیمی که به واسطه بروز این فرم از سندرم تولید می شود را اندازه گیری میکند.بیوپسی پوست: در این تست مقداری نمونه پوستی گرفته و در زیر میکروسکپ مورد بررسی قرار می گیرد. این تست به تشخیص ناهنجاریهایی در ساختار فیبری پوست مفید خواهد بود .اولتراسوند قلبی: بررسی به منظور تشخیص پرولاپس میترال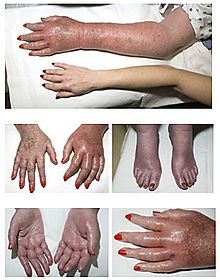

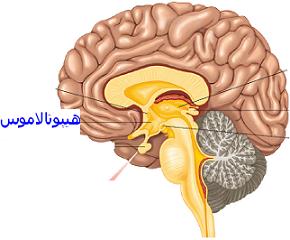
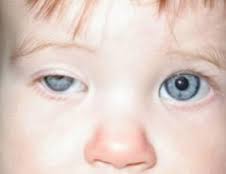
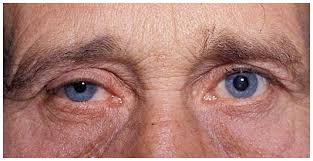 سندرم هورنر ،اختلالی است که به ندرت جمعیت عمومی با آن مواجه میشوند و شاید در هر شرایط سنی رخ دهد، شیوع بیماری در هر دو جنس یکسان است. در جمعیت مورد مطالعه شیوع این بیماری 421 در 100000 نفر در افراد زیر 19 سال و 1 در 6250نفر در حاملین این بیماری تخمین زده شده است.علت بیماری سندرم هورنر یک اختلال عصبی که حاصل قطع شدن عصب فیبر که از قسمت مغز تا صورت و چشمها ادامه دارد می باشد ،شرایط متفاوتی منجر به ایجاد این وضعیت می شوند و علل آن شامل: نامشخص، ضربه، تومور مغزی ،میگرن، دردهای خوشه ای سر، پرکاری تیروئید در سطع وسیع، سرطان ریه.علایم ناشی از بیماری علائم بیماری از سندرم هورنر به صورت خاص است یعنی یک مجموعه سه تائی از علائمی که یک طرف از صورت را تحت تأثیر قرار می دهد سه علائم مذبور عبارتند از: کم شدن عرق، افتادگی یک پلک، تنگی حدقه چشم. ارزیابی بالینی از افراد مبتلا برای شناسائی وضع موجود مناسب هستند. آزمایشات نورولوژی و شرح حال شاید در تأیید تشخیص این بیماری کمک کنند. سی تی اسِکن قفسه سینه، سی تی اسِکن مغز، رگ نگاری مغزی، نمونه برداری مایع نخاعی شاید برای بررسی سندرم هورنر انجام گیرد.روش تشخیص تشخیص به صورت بالینی بوده و از روی علائم و نشانه ها قابل تشخیص است. ممکن است استفاده از تصویر برداری و یا نوار عصبی و عضلانی برای افزایش اطلاعات و تایید نهایی استفاده شود.درمان نوع اولیه که علت مشخص ندارد تا به امروز درمان نداشته اما در انواع ثانویه و ثالثیه درمان در شرایط اکتسابی به سوی ریشه کنی علت به وجود آورنده بیماری سوق داده میشود . مراقبت های لازمحمایت روحی و روانی بیمار لازم می باشد. در خصوص هریک از مشکلات به وجود آمده نیز درمان مربوطه صورت میگیرد. از آنجایکه درمان قطعی بیماری تا به حال میسر نمی باشد لذا استفاد از تجهیزات کمی در جهت افزایش سطح زندگی بیمار مهم است.پیش آگهیپیش آگهی این بیماری به علت زمینه ای سندروم بستگی دارد. در صورت مادرزادی بودن امکان درمان قطعی وجود ندارد ولی اگر بصورت زمینه ای باشد معمولا با رفع علل به وجود آورنده علایم بیماری نیز تقلیل می یابد.
سندرم هورنر ،اختلالی است که به ندرت جمعیت عمومی با آن مواجه میشوند و شاید در هر شرایط سنی رخ دهد، شیوع بیماری در هر دو جنس یکسان است. در جمعیت مورد مطالعه شیوع این بیماری 421 در 100000 نفر در افراد زیر 19 سال و 1 در 6250نفر در حاملین این بیماری تخمین زده شده است.علت بیماری سندرم هورنر یک اختلال عصبی که حاصل قطع شدن عصب فیبر که از قسمت مغز تا صورت و چشمها ادامه دارد می باشد ،شرایط متفاوتی منجر به ایجاد این وضعیت می شوند و علل آن شامل: نامشخص، ضربه، تومور مغزی ،میگرن، دردهای خوشه ای سر، پرکاری تیروئید در سطع وسیع، سرطان ریه.علایم ناشی از بیماری علائم بیماری از سندرم هورنر به صورت خاص است یعنی یک مجموعه سه تائی از علائمی که یک طرف از صورت را تحت تأثیر قرار می دهد سه علائم مذبور عبارتند از: کم شدن عرق، افتادگی یک پلک، تنگی حدقه چشم. ارزیابی بالینی از افراد مبتلا برای شناسائی وضع موجود مناسب هستند. آزمایشات نورولوژی و شرح حال شاید در تأیید تشخیص این بیماری کمک کنند. سی تی اسِکن قفسه سینه، سی تی اسِکن مغز، رگ نگاری مغزی، نمونه برداری مایع نخاعی شاید برای بررسی سندرم هورنر انجام گیرد.روش تشخیص تشخیص به صورت بالینی بوده و از روی علائم و نشانه ها قابل تشخیص است. ممکن است استفاده از تصویر برداری و یا نوار عصبی و عضلانی برای افزایش اطلاعات و تایید نهایی استفاده شود.درمان نوع اولیه که علت مشخص ندارد تا به امروز درمان نداشته اما در انواع ثانویه و ثالثیه درمان در شرایط اکتسابی به سوی ریشه کنی علت به وجود آورنده بیماری سوق داده میشود . مراقبت های لازمحمایت روحی و روانی بیمار لازم می باشد. در خصوص هریک از مشکلات به وجود آمده نیز درمان مربوطه صورت میگیرد. از آنجایکه درمان قطعی بیماری تا به حال میسر نمی باشد لذا استفاد از تجهیزات کمی در جهت افزایش سطح زندگی بیمار مهم است.پیش آگهیپیش آگهی این بیماری به علت زمینه ای سندروم بستگی دارد. در صورت مادرزادی بودن امکان درمان قطعی وجود ندارد ولی اگر بصورت زمینه ای باشد معمولا با رفع علل به وجود آورنده علایم بیماری نیز تقلیل می یابد. 
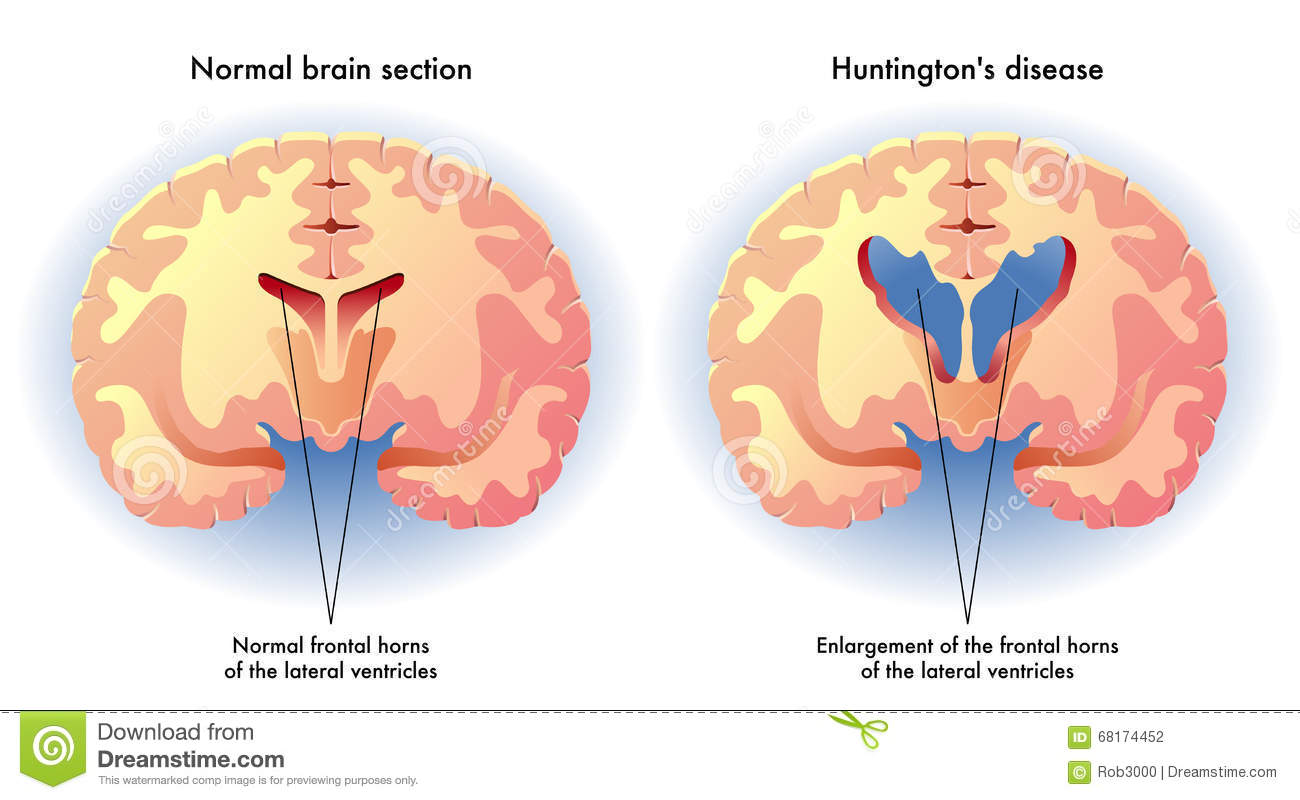 بروز این بیماری 2 تا 6 مورد از هر 000،100 نفر در سال میباشد میزان بروز در مردان و زنان برابر است. تقریبا 80 درصد بیماران نوجوان، ژن HD جهش یافته را از پدر به ارث می برند. تقریبا 3/1بیماران با اختلالات روانی تظاهر میکنند و دو سوم بیماران با ترکیبی از اختلالات شناختی و حرکتی مراجعه می کنند. علت بیماری هانتینگتون، نوعی اختلال تحلیل برنده عصبی اتوزومی غالب است که در تمام نژادها به چشم می خورد و به علت جهشهایی در ژن HD ایجاد میشود. این ژن حاوی یک توالی تکرارشونده سه نوکلئوتیدی(CAG)است که برای تشخیص بیماری هانتینگتون به کار میرود. در این بیماری هسته دم دار تالاموس، ساقه مغز و قسمت های دیگری از مغز آتروفی میگردد .علایم ناشی از بیماری هانتینگتون با اختلالات پیشرونده حرکتی، شناختی و روانی مشخص می شود. اختلالات حرکتی شامل حرکات ارادی و نیز غیرارادی می شوند. در ابتدا این حرکات به میزان ناچیزی در فعالیتهای روزانه مداخله می کنند، اما با پیشرفت بیماری، عموما ناتوان کننده می شوند. علایم مشخصه این بیماری ،تکان ها و حرکات غیرعادی، اختلال در تکلم، اختلال در تعقل و حالات عاطفی است. علایم بیماری عبارتند از:تحلیل رفتن جسمی و روانیبی حالی و بیتفاوتی(آپاتی)افسردگی یا هیجان پذیریاختلال حسیپیچ و تاب بی اراده دست و پاعدم تعادلحرکات ناموزون صورتچرخاندن زیاد لب به دور دهانصدا درآوردن با لب هاصحبت کردن غیرعادی همراه با فشار و صداهای انفجار آمیز.روش تشخیص یافته های حاصل اسکن مغز نشان دهنده تحلیل بافتی در مغز بوده و تصویربرداری با ام. ار.ای نیز کمک کننده است. آزمایشات ژنتیکی تایید کننده نهایی بیماری می باشد .درمان در حال حاضر ،هیچ درمان علاج دهنده ای برای بیماری هانتینگتون وجود ندارد. درمان بر مراقبت حمایتی و نیز اداره دارویی مشکلات رفتاری و عصبی متمرکز است. با پیشرفت کره بستری کردن در آسایشگاهها لازم میشود. علایم بیخوابی، اضطراب، و افسردگی را میتوان با مصرف بنزودیازپینها و ضدافسردگیها رفع کرد. علایم عصبی را میتوان با داروهای آنتی سایکوتیک پرقدرت یا آنتاگونیستهای سروتونین، دوپامین درمان کرد. مشاوره ژنتیک مهمترین مداخله میباشد .مراقبت های لازم افسردگی شدید یکی از مشکلات عمده در بیماران می باشد که نیازمند توجه بیشتر به بیمار است. بیمار در معرض ناتوانی جسمی برای انجام کارهای روزمره، احتمال آسیب به خود یا دیگران، افزایش خطر عفونت می باشد . پیش آگهی سیر این بیماری پیشرونده بوده و معمولاً 15 تا 20 سال بعد از تشخیص منجر به مرگ بیمار می شود. خودکشی در این بیماری شایع است.
بروز این بیماری 2 تا 6 مورد از هر 000،100 نفر در سال میباشد میزان بروز در مردان و زنان برابر است. تقریبا 80 درصد بیماران نوجوان، ژن HD جهش یافته را از پدر به ارث می برند. تقریبا 3/1بیماران با اختلالات روانی تظاهر میکنند و دو سوم بیماران با ترکیبی از اختلالات شناختی و حرکتی مراجعه می کنند. علت بیماری هانتینگتون، نوعی اختلال تحلیل برنده عصبی اتوزومی غالب است که در تمام نژادها به چشم می خورد و به علت جهشهایی در ژن HD ایجاد میشود. این ژن حاوی یک توالی تکرارشونده سه نوکلئوتیدی(CAG)است که برای تشخیص بیماری هانتینگتون به کار میرود. در این بیماری هسته دم دار تالاموس، ساقه مغز و قسمت های دیگری از مغز آتروفی میگردد .علایم ناشی از بیماری هانتینگتون با اختلالات پیشرونده حرکتی، شناختی و روانی مشخص می شود. اختلالات حرکتی شامل حرکات ارادی و نیز غیرارادی می شوند. در ابتدا این حرکات به میزان ناچیزی در فعالیتهای روزانه مداخله می کنند، اما با پیشرفت بیماری، عموما ناتوان کننده می شوند. علایم مشخصه این بیماری ،تکان ها و حرکات غیرعادی، اختلال در تکلم، اختلال در تعقل و حالات عاطفی است. علایم بیماری عبارتند از:تحلیل رفتن جسمی و روانیبی حالی و بیتفاوتی(آپاتی)افسردگی یا هیجان پذیریاختلال حسیپیچ و تاب بی اراده دست و پاعدم تعادلحرکات ناموزون صورتچرخاندن زیاد لب به دور دهانصدا درآوردن با لب هاصحبت کردن غیرعادی همراه با فشار و صداهای انفجار آمیز.روش تشخیص یافته های حاصل اسکن مغز نشان دهنده تحلیل بافتی در مغز بوده و تصویربرداری با ام. ار.ای نیز کمک کننده است. آزمایشات ژنتیکی تایید کننده نهایی بیماری می باشد .درمان در حال حاضر ،هیچ درمان علاج دهنده ای برای بیماری هانتینگتون وجود ندارد. درمان بر مراقبت حمایتی و نیز اداره دارویی مشکلات رفتاری و عصبی متمرکز است. با پیشرفت کره بستری کردن در آسایشگاهها لازم میشود. علایم بیخوابی، اضطراب، و افسردگی را میتوان با مصرف بنزودیازپینها و ضدافسردگیها رفع کرد. علایم عصبی را میتوان با داروهای آنتی سایکوتیک پرقدرت یا آنتاگونیستهای سروتونین، دوپامین درمان کرد. مشاوره ژنتیک مهمترین مداخله میباشد .مراقبت های لازم افسردگی شدید یکی از مشکلات عمده در بیماران می باشد که نیازمند توجه بیشتر به بیمار است. بیمار در معرض ناتوانی جسمی برای انجام کارهای روزمره، احتمال آسیب به خود یا دیگران، افزایش خطر عفونت می باشد . پیش آگهی سیر این بیماری پیشرونده بوده و معمولاً 15 تا 20 سال بعد از تشخیص منجر به مرگ بیمار می شود. خودکشی در این بیماری شایع است.
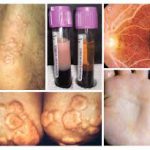 شیوع و همه گیر شناسی نزدیک به 5% از کل جمعیت از لحاظ 2E2/apoE هوموزیگوت هستند اما فقط بخش کوچکی از این افراد دچار این بیماری میشوند .علت بیماری نقص ژنتیکی باعث این بیماری است. این نقص از تجمع ذرات بزرگ لیپوپروتئینی که حاوی کلسترول و تری گلیسرید که خود نوعی چربی است به وجود می آید. این بیماری با نقص در ژن آپولیپو پروتئین E در ارتباط است. در بیشتر موارد، یک عامل اضافی شناسایی دیگر در بروز هیپرلیپوپروتئینمی دخیل است. شایع ترین این عوامل رژیم های پرکالری – پر چربی، دیابت، چاقی ،هیپرلیپیدمی می باشند که در بیشتر موارد هیپرلیپیدمی فامیلی و مرکب(FCHL)یا هیپرکلسترولمی فامیلی(FH)است. جهش های نادری در apoE باعث شک لگیری اشکال غالب FDBL می شوند؛ در این موارد هیپرلیپیدمی به طور کامل، در شرایط هتروزیگوت، بروز می نماید.علایم ناشی از بیماری بیماران دچار FDBL معمولاً در جوانی دچار گزانتوم می شوند و بیماری های عروق کرونری و محیطی زودرس پیدا می کنند بیماری به ندرت در زنان ،پیش از یائسگی بروز می کند. دو نوع ششخص از گزانتوم ها در بیماران دچار FDBL دیده میشوند: –Tubero eruptive و گزانتوم های کف دست. گزانتوم هایی که به صورت خوشه هایی از ضایعات پوستی برجسته روی آرنجها زانوها یا باسن ها شروع شده و میتوانند به اندازۀ دانههای کوچک انگور برسند. گزانتوم کف دست(که به آن استریاتاپالماریس هم گفته می شود)تغییر رنگهای نارنجی مایل به زرد کف دست هستند.روش تشخیصرویکرد کلاسیک، تشخیص این اختلال استفاده از الکتروفورز لیپوپروتئین ها است؛ در FDBL، لیپوپروتئی نهای باقی مانده به صورت یک باند β پهن تجمع می کنند، روش ارجح برای تأیید تشخیص FDBL اندازهگیری VLDL- 3با استفاده از اولتراسانتریفوژ و مشخص کردن نسبت VLDL-C به کل تری گلیسرید پلاسما است؛ نسبت 30%> نشاندهندۀ FDBL است. آزمایشاتی که ممکن است برای تشخیص این بیماری انجام شود عبارتند از:تست ژنتیکی برای آپولیپو پروتئیناسترس تست قلبکلسترول تامتری گلیسیریدتست( VLDL)لیپوپروتئینی با حجم بسیار کمدرمان افراد دچار FCHL را باید به صورت تهاجمی درمان کرد چرا که خطر CHD زودرس در آنها به طور مشخص بالا است .کاهش مصرف خوراکی چربی اشباع و کربوهیدرات ساده، ورزش هوازی و کاهش وزن اثرات مفیدی روی پروفایل لیپید دارد. بیماران دیابتی را باید به صورت تهاجمی درمان کرد تا سطح گلوکز خون در حد مطلوب بماند. بیشتر بیماران FCHL نیاز به داروهای ضد چربی دارند تا لیپوپروتئین هایشان به حد مطلوب برسد. در زنان یائسه، دیس لیپیدمی به جایگزینی هورمونی استروژن پاسخ میدهد و درمان دارویی ترکیبی گاهی اوقات مورد نیاز خواهد بود.مراقبت های لازم درمان زود هنگام و اجتناب از سایر عوامل خطرساز برای بیماری های عروقی )مانند سیگار کشیدن( برای جلوگیری از حملات قلبی زودرس، سکته مغزی و مسدود شدن رگهای خونی بسیار مهم و ضروری هستند.پیش آگهی سایر شرایط متابولیک که می توانند هیپرلیپیدمی را بدتر کنند باید فعالانه درمان شوند. بیماران FDBL به طور تیپیک خیلی خوب به رژیم غذایی پاسخ میدهند کاهش وزن و رژیم های کم کلسترول کم چربی میتواند پاسخ خوب در این بیماران ایجاد نمایند .مصرف الکل باید قطع شود .پیش آگهی به پایبندی و پاسخ فردی به برنامۀ درمانی بستگی دارد. هدف درمان پیشگیری از عوارض ثانویه آن از جمله بی ماریهای قلبی و عروقی است.
شیوع و همه گیر شناسی نزدیک به 5% از کل جمعیت از لحاظ 2E2/apoE هوموزیگوت هستند اما فقط بخش کوچکی از این افراد دچار این بیماری میشوند .علت بیماری نقص ژنتیکی باعث این بیماری است. این نقص از تجمع ذرات بزرگ لیپوپروتئینی که حاوی کلسترول و تری گلیسرید که خود نوعی چربی است به وجود می آید. این بیماری با نقص در ژن آپولیپو پروتئین E در ارتباط است. در بیشتر موارد، یک عامل اضافی شناسایی دیگر در بروز هیپرلیپوپروتئینمی دخیل است. شایع ترین این عوامل رژیم های پرکالری – پر چربی، دیابت، چاقی ،هیپرلیپیدمی می باشند که در بیشتر موارد هیپرلیپیدمی فامیلی و مرکب(FCHL)یا هیپرکلسترولمی فامیلی(FH)است. جهش های نادری در apoE باعث شک لگیری اشکال غالب FDBL می شوند؛ در این موارد هیپرلیپیدمی به طور کامل، در شرایط هتروزیگوت، بروز می نماید.علایم ناشی از بیماری بیماران دچار FDBL معمولاً در جوانی دچار گزانتوم می شوند و بیماری های عروق کرونری و محیطی زودرس پیدا می کنند بیماری به ندرت در زنان ،پیش از یائسگی بروز می کند. دو نوع ششخص از گزانتوم ها در بیماران دچار FDBL دیده میشوند: –Tubero eruptive و گزانتوم های کف دست. گزانتوم هایی که به صورت خوشه هایی از ضایعات پوستی برجسته روی آرنجها زانوها یا باسن ها شروع شده و میتوانند به اندازۀ دانههای کوچک انگور برسند. گزانتوم کف دست(که به آن استریاتاپالماریس هم گفته می شود)تغییر رنگهای نارنجی مایل به زرد کف دست هستند.روش تشخیصرویکرد کلاسیک، تشخیص این اختلال استفاده از الکتروفورز لیپوپروتئین ها است؛ در FDBL، لیپوپروتئی نهای باقی مانده به صورت یک باند β پهن تجمع می کنند، روش ارجح برای تأیید تشخیص FDBL اندازهگیری VLDL- 3با استفاده از اولتراسانتریفوژ و مشخص کردن نسبت VLDL-C به کل تری گلیسرید پلاسما است؛ نسبت 30%> نشاندهندۀ FDBL است. آزمایشاتی که ممکن است برای تشخیص این بیماری انجام شود عبارتند از:تست ژنتیکی برای آپولیپو پروتئیناسترس تست قلبکلسترول تامتری گلیسیریدتست( VLDL)لیپوپروتئینی با حجم بسیار کمدرمان افراد دچار FCHL را باید به صورت تهاجمی درمان کرد چرا که خطر CHD زودرس در آنها به طور مشخص بالا است .کاهش مصرف خوراکی چربی اشباع و کربوهیدرات ساده، ورزش هوازی و کاهش وزن اثرات مفیدی روی پروفایل لیپید دارد. بیماران دیابتی را باید به صورت تهاجمی درمان کرد تا سطح گلوکز خون در حد مطلوب بماند. بیشتر بیماران FCHL نیاز به داروهای ضد چربی دارند تا لیپوپروتئین هایشان به حد مطلوب برسد. در زنان یائسه، دیس لیپیدمی به جایگزینی هورمونی استروژن پاسخ میدهد و درمان دارویی ترکیبی گاهی اوقات مورد نیاز خواهد بود.مراقبت های لازم درمان زود هنگام و اجتناب از سایر عوامل خطرساز برای بیماری های عروقی )مانند سیگار کشیدن( برای جلوگیری از حملات قلبی زودرس، سکته مغزی و مسدود شدن رگهای خونی بسیار مهم و ضروری هستند.پیش آگهی سایر شرایط متابولیک که می توانند هیپرلیپیدمی را بدتر کنند باید فعالانه درمان شوند. بیماران FDBL به طور تیپیک خیلی خوب به رژیم غذایی پاسخ میدهند کاهش وزن و رژیم های کم کلسترول کم چربی میتواند پاسخ خوب در این بیماران ایجاد نمایند .مصرف الکل باید قطع شود .پیش آگهی به پایبندی و پاسخ فردی به برنامۀ درمانی بستگی دارد. هدف درمان پیشگیری از عوارض ثانویه آن از جمله بی ماریهای قلبی و عروقی است.